FeO + CO → Fe + CO2↑ là phản ứng oxi hóa - khử. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng: FeO + CO → Fe + CO2↑
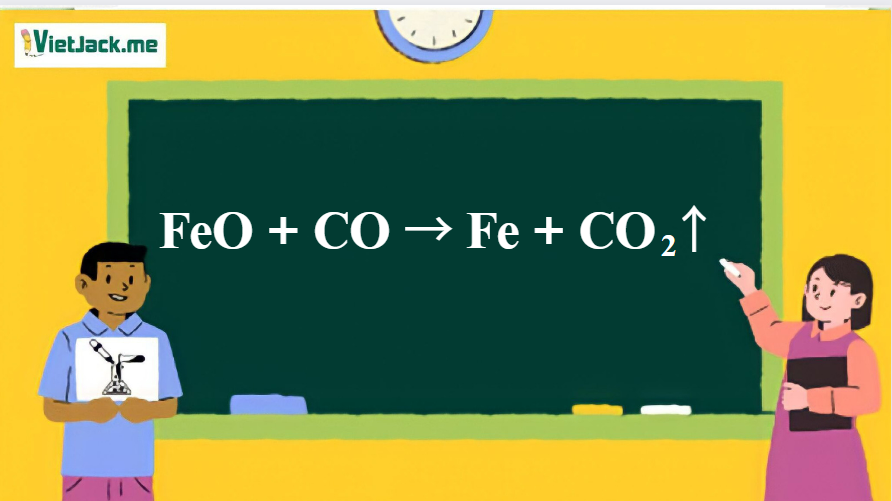
1. Phương trình phản ứng giữa FeO và CO
FeO + CO → Fe + CO2↑
2. Điều kiện phản ứng
- Nhiệt độ: 700-800°C
3. Hiện tượng nhận biết phản ứng
- Phản ứng có khí CO2 thoát ra
4. Bản chất của các chất tham gia phản ứng
4.1 Bản chất của FeO
- FeO thể hiện tính oxi - hóa
4.2 Bản chất của CO
- Trong phản ứng trên, CO đóng vai trò là chất khử
5. Tính chất hóa học của FeO
- Mang đầy đủ tính chất hóa học của oxit bazo.
- Là chất vừa có tính oxi hóa, vừa có tính khử
5.1 Tính oxit bazơ
FeO tác dụng với dung dịch axit: HCl, H2SO2 loãng
FeO + 2HCl → FeCl2 + H2
FeO + H2SO4 loãng → FeSO4 + H2O
5.2 Tính oxi hóa
- Tác dụng với chất khử như H2, CO, Al, C…
FeO + H2 → Fe + H2O
FeO + CO → Fe + CO2
3FeO + 2Al → Al2O3 + 3Fe
5.3 Tính khử
- FeO là chất khử khi tác dụng với các chất có tính oxi hóa mạnh:
3FeO + 10HNO3 loãng → 3Fe(NO3)3 + NO + 5H2O
2FeO + 4H2SO4 (đặc) → Fe2(SO4)3 + SO2 + 4H2O
6. Tính chất hóa học của CO
6.1 CO là oxit trung tính
– Ở điều kiện thường CO không phản ứng với nước, axit, bazơ.
6.2 CO là chất khử
– Ở nhiệt độ cao, CO khử được nhiều oxit kim loại
CO + CuO → CO2 + Cu
2CO + Fe3O4 → 3Fe + 2CO2
2CO + O2 → 2CO2
7. Ứng dụng của FeO
Chúng được sử dụng làm chất trợ chảy và tạo màu cho men. FeO là chất rắn màu đen, không tan trong nước, nhiệt độ nóng chảy 1370 °C. FeO là một chất nóng chảy mạnh vì vậy nó được sử dụng làm chất trợ chảy, có thể thay thế cho CaO và PbO.
8. Bạn có biết
Ở nhiệt độ cao, CO có thể khử được nhiều oxit kim loại về kim loại (CuO, Fe2O3, ZnO,...)
9. Ví dụ minh họa
Ví dụ 1: Cách nào sau đây có thể dùng để điều chế FeO ?
A. Dùng CO khử Fe2O3 ở 500°C.
B. Nhiệt phân Fe(OH)2 trong không khí.
C. Nhiệt phân Fe(NO3)2
D. Đốt cháy FeS trong oxi.
Hướng dẫn giải
Để điều chế FeO, người ta khử Fe2O3 bằng CO ở nhiệt độ cao
Đáp án : A
Ví dụ 2: Mệnh đề không đúng là:
A. Fe2+ oxi hoá được Cu.
B. Fe khử được Cu2+ trong dung dịch.
C. Fe3+ có tính oxi hóa mạnh hơn Cu2+.
D. Tính oxi hóa của các ion tăng theo thứ tự: Fe2+, H+, Cu2+, Ag+
Hướng dẫn giải
Trong dãy điện hóa, thứ tự các cặp được sắp xếp như sau Fe2+/Fe , H+/H2, Cu2+ /Cu, Fe3+ / Fe2+
Theo quy tắc α thì Fe2+ chỉ oxi hóa được các kim loại đứng trước nó, không oxi hóa được Cu.
Đáp án : A
Ví dụ 3: Chất nào dưới đây phản ứng với Fe tạo thành hợp chất Fe(II) ?
A. Cl2 B. dung dịch HNO3 loãng
C. dung dịch AgNO3 dư D. dung dịch HCl đặc
Hướng dẫn giải
Đáp án : D